Na 2 maanden klinische ervaring met coronavirus disease 2019 (COVID-19) leren we steeds meer over deze ziekte. Voortschrijdend inzicht laat zien dat het Severe Acute Respiratory Syndrome Corona Virus 2 (SARS-CoV-2) een toegenomen trombogeniciteit veroorzaakt. En dat merken we ook in de dagelijkse praktijk: we zien patiënten met longembolieën en horen over versneld opstollen van dialysefilters. Dat geeft ons stof tot nadenken over onderwerpen zoals tromboseprofylaxe en D-dimeer bepalingen. Na de uitzending van Jinek van 1 mei mogen we ook het middel resveratrol aan deze lijst met onderwerpen toevoegen.(1,2) Of dit middel daadwerkelijk de morbiditeit en mortaliteit van COVID-19 patiënten beïnvloedt, is nog onbekend. Daarom hebben wij aan de hand van een aantal praktische vragen een uiteenzetting voor jullie gemaakt over wat er wél bekend is in de literatuur over de toegenomen stollingsneiging bij COVID-19.
Key points
- In meerdere kleine studies blijkt dat veneuze trombo-embolieën (VTE) significant meer voorkomen bij COVID-19 patiënten, zowel op de IC, de verpleegafdeling en in ambulante setting.
- Risicofactoren voor VTE in COVID-19 patiënten zijn oudere leeftijd, lymfopenie en (licht) verlengde stollingstijden.
- Micro-vasculaire inflammatie en -trombose lijken een belangrijk onderdeel uit te maken van het pathofysiologische mechanisme dat betrokken is bij het ontstaan van VTE in COVID-19 patiënten.
- In een enkele studie wordt gesuggereerd dat het ophogen van de dosering tromboseprofylaxe een verbetering geeft in stollingswaarden, maar data naar patiëntgeoriënteerde eindpunten (zoals mortaliteit) ontbreken.
- Er lijkt een associatie te bestaan tussen de hoogte van de D-dimeer, optreden van VTE en mortaliteit bij COVID-19 patiënten. Wellicht gaat in de toekomst D-dimeer bepaling bij opname gebruikt worden bij de risicostratificatie voor mortaliteit.
Hoe vaak komen veneuze trombo-embolieën bij COVID-19 voor?
Chinese studies uit februari en maart beschrijven verstoorde stollingsparameters en verhoogd D-dimeer in het opnamelab van patiënten met COVID-19.(3-7) In deze studies wordt gesuggereerd dat er, met name bij patiënten met slechtere uitkomst, sprake is van hypercoagulabiliteit en ‘disseminated intravasculair coagulation’ (DIC). Over de incidentie van veneuze trombo-embolieën (VTE) was toen, op enkele case reports na, weinig bekend.(8-10)
Nederlands onderzoek
Gelukkig weten we hier inmiddels in de maand april al iets meer over. Te beginnen met de incidentie op eigen bodem: de studie van Klok et al.(11) Het betreft een observationele studie onder 184 COVID-19 bewezen patiënten, verricht op de Intensive Care (IC) in het LUMC, Erasmus MC en Amphia ziekenhuis. Standaard werd bij elke patiënt 2850 IE tot 5700 IE nadroparine (0.3-0.6 cc fraxiparine) per dag gegeven. Toch was de gecombineerde incidentie voor longembolie (LE), diep veneuze trombose (DVT), ischemisch cerebrovasculair incident (iCVA), myocardinfarct en systemische arteriële embolieën bij elkaar 31% (95% confidence interval (CI) 20-41%). Op basis van klinische verdenking werd CT-pulmonaal angiografie (CTPA) en een echo DVT verricht. Hierbij had 27% van de patiënten een LE of DVT. Dat zijn meer VTEs dan je in een gemiddelde IC populatie met tromboseprofylaxe verwacht (≈8-13% van de patiënten).(12,13) In een recente heranalyse van deze populatie, waarbij de mediane follow-up tijd 7 dagen langer was, vonden ze zelfs een cumulatieve incidentie voor trombo-embolieën van 49% (95% CI 41-57%).(14)
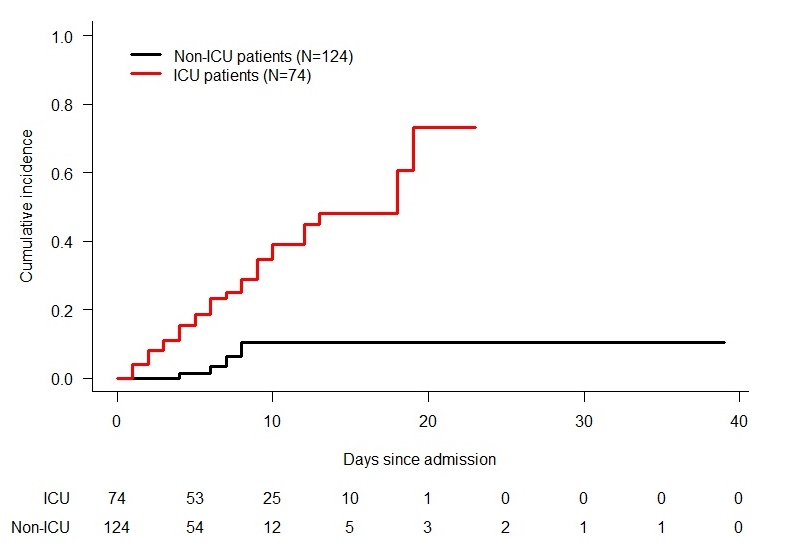
In de studie van Middeldorp et al (n=198) in het Amsterdam UMC is de VTE-incidentie bij COVID-19 patiënten 17% na een mediane tijd van 5 dagen.(15) Hiervan was 11% symptomatisch. De cumulatieve incidentie na 14 dagen loopt op tot 34%. Op de IC was dit aantal hoger (48% na 14 dagen) dan op de verpleegafdeling (10% na 14 dagen; zie ook figuur 1 hieronder). Het krijgen van een VTE was geassocieerd met toegenomen mortaliteit (adjusted hazard ratio (aHR) 2.9; 95% CI 1.02-8.0). Alle patiënten in deze studie kregen tromboseprofylaxe. Voor patiënten op de afdeling 1 dd 2850 IE nadroparine s.c., en een dubbele dosis voor IC-patiënten en patiënten ≥100 kg. Het grootste verschil met de studie van Klok et al is dat bij een gedeelte van de studiepopulatie de diagnostiek naar DVT door middel van screening plaatsvond, in plaats van alleen op indicatie. Diagnostiek naar LE vond alleen plaats op indicatie.
Onderzoek uit andere landen
De resultaten uit Nederland zijn vergelijkbaar met data uit China en Frankrijk. Op de IC in China (n=81) wordt een incidentie van 25% VTE gevonden.(16) Hiervan overleed uiteindelijk 40%. Eén belangrijk verschil: in deze groep gaven ze geen standaard tromboseprofylaxe, waarschijnlijk door de lagere incidentie van VTE in de Aziatische populatie vergeleken met andere bevolkingsgroepen.(17) In Lille, Frankrijk, is de incidentie van LE op hun COVID-IC (n=107) 20.6% versus 6.1% in hun IC-populatie een jaar geleden.(18) Daarbij kregen alle patiënten tromboseprofylaxe of therapeutische antistolling. Helms et al, ook van Franse bodem, beschreven in hun prospectieve IC-studie een incidentie van trombotische complicaties van 43% (64/150).(19) Mediane duur van IC-opname tot diagnose was 5,5 dagen. Hiervan was 16.7% een LE, maar ook andere arteriële en veneuze trombo-embolieën werden beschreven (zoals iCVA’s en mesenteriaal ischemie). Na matchen met non-COVID-19 ARDS-patiënten is het aantal trombo-embolieën in de COVID-19 groep hoger (11.7% vs. 4.8%, OR 2.6 [95% CI 1.1-6.1], p=0.035).
De meeste van de hierboven genoemde studies verrichtten diagnostiek alleen op indicatie. Risico hiervan is onderschatting van de ware incidentie van VTE. Een kleine studie ondersteunt deze theorie. In de populatie van 2 ICs (n=26) kreeg 69% van de patiënten al therapeutische doseringen low molecular weight heparine (LMWH) en de rest profylactische doseringen. Een screenende echo werd in de eerste 3 dagen na opname, of, indien deze negatief was, op dag 7 van opname verricht. Alsnog bleek 69% van hun patiënten een perifere VTE te hebben. Dit is 100% van de patiënten die profylactisch LMWH kregen en 56% van de patiënten met therapeutisch LMWH. Uit de CTPA die zij op indicatie bij respiratoir falen verrichtten, bleek 23% een LE te hebben.(20) Dan wordt men toch wel nieuwsgierig welke doseringen LMWH ze hanteerden: helaas geven ze dit niet prijs.
Ook bij klinische, niet-IC-behoeftige COVID-19 patiënten zien we een toegenomen VTE-incidentie. In een ziekenhuis in Lombardije, Italië, hebben ze bij 30 COVID-19 patiënten vanwege verdenking DVT een echo gemaakt: 53% had een DVT.(21) In vergelijking met 24 patiënten die een jaar daarvoor een echo ondergingen, had maar 21% een DVT. In de studie van Lodigiani et al uit Milaan (n=388) ligt de incidentie VTE lager: 8% van de patiënten kreeg een arteriële of veneuze trombo-embolie.(22) Dit vertaalde zich in een cumulatieve incidentie van 21%, waarvan 27.6% op de IC en 6.4% op de verpleegafdeling. 56% van deze patiënten gebruikten profylactische of therapeutische antistolling. Ook in deze studie werd alleen diagnostiek op indicatie verricht. Opvallend is dat 50% van de VTE werd gediagnosticeerd binnen 24 uur na opname.

Het artikel van Cattaneo et al staat helemaal in contrast met eerder genoemde hoge incidenties. Ook gevestigd te Milaan, laten zij zien dat op hun COVID-19 verpleegafdeling, waar iedereen tromboseprofylaxe krijgt, 0% DVTs werden gevonden.(23) Zelfs in een subgroep die screenend een echo onderging werden geen DVTs gevonden. Gezien de tegenstrijdigheid van deze studieresultaten in het licht van alle andere data die we hebben verzameld over de incidentie van VTE, laten wij deze studie in onze conclusie buiten beschouwing.
Tot slot nog twee studies over CTPA bij COVID-19 patiënten uit Frankrijk van Leonard-Lorant et al en Grillet et al. Zij verrichtten bij respectievelijk 11% (106/961) en 5% (100/2003) van hun COVID-19 populatie een CTPA.(24,25) In deze twee studies werd bij 30% en 23% van de patiënten een LE gevonden (versus 11% LE bij niet-COVID-19 patiënten, Leonard-Lorant et al). Verder uitgesplitst is dit in de groep niet-IC-patiënten: 14% en 10% LE en bij IC-patiënten 50% en 44%.
Kanttekening bij deze percentages is dat dit de incidentie betreft van alle patiënten die een CTPA kregen, en niet over het totaal aantal opgenomen COVID-19 patiënten. Bij gebrek aan data over het aantal COVID-19 patiënten in deze subgroepen zonder CTPA kunnen we incidentie in deze afzonderlijke populaties helaas ook niet voor jullie uitrekenen. Wél over de hele populatie COVID-19 patiënten die in deze studies de revue passeren. Dit komt neer op een incidentie van 3.3% en 1.1% in de studies van respectievelijk Leonard-Lorant en Grillet. Normaal gesproken ligt deze incidentie in de algemene bevolking rond de 0.07%.(26,27)
Samengevat
- Incidentie van VTE bij COVID-19 IC-patiënten varieert van 8% tot 39%, met een cumulatieve incidentie na 14 dagen tot wel 49%, ondanks profylactische, maar in sommige gevallen ook therapeutische toediening van LMWH.
- Voor klinische niet-IC-patiënten is de incidentie van VTE 3-4%, met een cumulatieve incidentie na 14 dagen tot 10%.
- Het krijgen van een VTE is geassocieerd met toegenomen mortaliteit.
Risicofactoren
In de eerder genoemde IC-studies wordt al gehint op mogelijke risicofactoren voor het ontwikkelen van een VTE. Hierbij worden de volgende risicofactoren beschreven:
- Oudere leeftijd (VTE: 68.4 jaar vs. niet-VTE: 57.1 jaar, P<0.001).(11,16)
- Lager lymfocytenaantal (0.8 vs. 1.3×109/L, P<0.001)
- Licht verlengde stollingstijden (APTT 39.9 vs. 35.6 sec., P=0.001, normale range 27-45 sec.).(16)
Verlengde stollingstijden waren geassocieerd met een toegenomen hazard op VTE (aHR 4.1, 95% CI 1.9-9.1). Dit zou kunnen wijzen op uitgebreidere inflammatie en coagulopathie in patiënten die uiteindelijk een VTE ontwikkelen en vormt meteen een brug naar onze volgende vraag.
Wat is het achterliggende pathofysiologische mechanisme?
We weten dat sepsis leidt tot hypercoagulabiliteit, we noemen dit ook wel tromboinflammatie.(28,29) Het beoogde effect hiervan is goed bedoeld van het lichaam, namelijk het insluiten van een pathogeen om verdere verspreiding te voorkomen. Dat kan echter uit de hand lopen, zoals bij DIC.(30) In de literatuur zien we dat dit ook voorkomt bij COVID-19 patiënten. Tang et al (n=183) beschrijft dat 71.4% van de non-survivors versus 0.6% van de survivors voldoet aan de DIC-criteria, wat meteen onderstreept dat dit geassocieerd is met verhoogde mortaliteit.(7)
Om in te gaan op de technische details:
- COVID-19, en dan met name bij een ernstig beloop, wordt gekenmerkt door een proinflammatoir cytokine profiel (verhoogd IL-1, IL-6, IL-8 en TNF-α).(31,32) In meerdere studies is aangetoond dat dit endotheel, monocyten en neutrofielen stimuleert tot toegenomen expressie van tissue factor (TF). TF leidt vervolgens tot activering van de ‘extrinsieke pathway’ van de stollingscascade.(33,34)
- In COVID-19 wordt toegenomen circulerende hoeveelheden van von Willebrand factor (VWF) aangetoond.(35,36) De toegenomen expressie van VWF kan aanleiding geven tot trombocyten-activatie en -aggregatie.(34,37)
- Daarnaast zijn er aanwijzingen voor endotheel-dysfunctie en -inflammatie.(38) Dat is niet geheel ondenkbaar, gezien de angiotensine converting enzyme-2 (ACE-2) receptor, die het virus gebruikt om de cel binnen te komen,(39) op vasculair glad spierweefsel en vasculaire endotheelcellen aanwezig lijken te zijn.(40,41)
- SARS-CoV-2 lijkt ook ACE-2 te downreguleren,(42) wat mogelijk verder bijdraagt aan de trombogeniciteit van het virus. Dit komt doordat ACE-2 geassocieerd is met immuunmodulerende, anti-inflammatoire eigenschappen(43-45) en actief angiotensine II omzet naar angiotensine 1-7.(46) En van angiotensine II is aangetoond dat het protrombotische eigenschappen heeft.(47)
- Verder zijn in kleine studies over long- en huidbiopten aanwijzingen gevonden dat complement-activatie een rol kan spelen in de pathogenese van COVID-19, tezamen met microvasculaire trombose, wat doet denken aan trombotische microangiopathie (TMA, waarvan de trombotische trombocytopenische purpura (TTP) een voorbeeld is).(48)
Dit komt overeen met de aanwijzingen die we krijgen uit de spaarzame post-mortem studies in SARS-CoV-2 patiënten. Men vindt hoofdzakelijk ‘diffuse alveolar damage’ (DAD) in combinatie met getromboseerde, geoccludeerde vaten.(49-51)
De observaties van het opnamelab bij COVID-19 patiënten(3-6,8,31,36,52,53) ondersteunen dat we bij de meeste COVID-19 patiënten niet te maken hebben met een klassieke DIC met verbruik van stollingsfactoren en verhoogde bloedingsneiging. Er lijkt met name sprake van microvasculaire inflammatie en -trombose dan wel van een ‘pulmonary intravasculair coagulation’ (PIC), wat mogelijk gezamenlijk verantwoordelijk is voor de toegenomen incidentie van VTE in deze populatie (figuur 2).(54,55) In dat geval hebben we het dus niet alleen over longembolieën, maar ook over longtrombose.(56)

Tromboseprofylaxe
Hierover is de informatie wat schaarser. In een Chinese studie was voor patiënten met een D-dimeer >3000 mcg/L en die tromboseprofylaxe gebruikten de 28 dagen-mortaliteit significant lager, vergeleken met patiënten die geen profylaxe kregen toegediend.(57) Over de hele groep gezien, met zowel een laag als hoog D-dimeer, maakte het geven van tromboseprofylaxe geen belangrijk verschil. Kanttekening hierbij is opnieuw dat dit een Aziatische populatie betreft waarbij de incidentie van VTE relatief laag is.(17)
Ranucci et al heeft aangetoond dat het ophogen van de standaard tromboseprofylaxe in zijn IC-populatie leidt tot daling van D-dimeer en fibrinogeen.(58) Dit suggereert dat een hogere dosering meer bereikt dan de standaard tromboseprofylaxe. Of dit daadwerkelijk een lagere incidentie van VTE en minder mortaliteit geeft, is nog niet aangetoond. Wel komt naar voren in de subanalyse van Klok et al., dat chronisch gebruik van therapeutische antistolling een lagere hazard op het ontwikkelen van trombo-embolieën oplevert (HR 0.29, 95% CI 0.091-0.92).(14) De hazard voor mortaliteit in deze subgroep verschilt echter niet (HR 0.79, 95% CI 0.35-1.8). Dit geeft weer extra informatie in de discussie over welke dosering LMWH voor deze COVID-19-IC-patiënten optimaal is.
Tegenwoordig wordt op Nederlandse ICs geadviseerd hoog profylactische doseringen LMWH te gebruiken.(59) Dit advies is uitgebracht op basis van de observatie dat ondanks normale doseringen tromboseprofylaxe er alsnog een verhoogde incidentie van VTE is bij COVID-19 IC patiënten.(58) Echter is de optimale dosering voor bepaalde subgroepen, zoals patiënten met obesitas, nog onbekend. Door het RIVM wordt op empirische gronden geadviseerd om bij alle patiënten die opgenomen worden met COVID-19 te starten met tromboseprofylaxe, onafhankelijk van hun risico op DVT.(60)
In het verlengde daarvan kun je je afvragen of we niet ook COVID-19 patiënten met risicofactoren op DVT in ambulante setting moeten behandelen met tromboseprofylaxe. Het feit dat in de studie van Lodigiani de helft van de VTEs binnen 24 uur na ziekenhuisopname gediagnosticeerd wordt,(22) doet vermoeden dat een belangrijk deel van de VTE al voor opname ontstaat. En hoe lang moeten we patiënten na ontslag van IC of uit het ziekenhuis door behandelen met tromboseprofylaxe? De meeste data over de incidentie van DVT, LE of VTE gezamenlijk gaan niet in op hoe lang patiënten al klachten hebben alvorens ze een VTE ontwikkelen. We wachten vooralsnog op studies die deze vragen beantwoorden.
D-dimeer
Over de toegevoegde waarde van de D-dimeer bepaling is iets meer bekend. In meerdere Chinese COVID-19 cohortstudies is het D-dimeer verhoogd (36% tot 46% van de patiënten)(53,61) en is het gemiddelde D-dimeer hoger in de groep die naar de IC gaat of overlijdt (niet-IC/survivors 500-600 mcg/L vs. IC/non-survivors 2100-5200 mcg/L).(3-7)
De hoogte van het D-dimeer in het opnamelab lijkt een onafhankelijke voorspeller te zijn voor mortaliteit (odds ratio 18.42, P=0.003).(5) Patiënten hebben op dat moment al zo’n 7 tot 10 dagen (mediaan) klachten.(4,31) Dit suggereert dat we wellicht, na validatiestudies, het D-dimeer bij opname kunnen gaan gebruiken in de risicostratificatie voor de mortaliteit in COVID-19 patiënten.
Lastiger is het om met behulp van het D-dimeer in de COVID-19 patiënten verdenking op VTE te baseren. In het kader van ongoing trombo-inflammatie lijkt in de groep als geheel het D-dimeer hoger te zijn. Er zijn een paar studies die verschillende afkapwaarden noemen. Cui et al geeft bij een afkapwaarde van 1500 mcg/L een sensitiviteit van 85%, specificiteit van 88.5%, negatief voorspellende waarde van 94.7% en positief voorspellende waarde van 70.8% voor VTE.(16) Bij een afkappunt van 3000 mcg/L is dit respectievelijk 70%, 96.7%, 90.8% en 87.5%. Met andere woorden, bij een afkapwaarde van 1500 mcg/L kunnen we een VTE bij COVID-19 patiënten het beste uitsluiten. De studie van Leonard-Lorant et al heeft voor alleen LE een afkapwaarde van 2660 mcg/L een sensitiviteit van 100% en een specificiteit van 67%.(25) Het gaat in deze studies om kleine aantallen (n=81 en n=106) en dit zijn geen validatiestudies.(16,25) Daarom blijft het RIVM voorlopig adviseren om de conventionele afkapwaardes voor het D-dimeer te gebruiken op basis van de YEARS criteria (>500 mcg/L indien positieve YEARS criteria, anders >1000 mcg/L) dan wel de leeftijd-afhankelijke D-dimeer (grens = 10 X leeftijd (mcg/L)).(60)
Daarnaast benoemt het RIVM in hun advies de mogelijkheid om het D-dimeer gedurende de opname te vervolgen. Bij waarden <1000 mcg/L adviseren zij profylactisch LWMH te continueren, maar bij waarden >2000-4000 mcg/L adviseren ze om te overwegen een CTPA te maken.(60)
Advies
Besef dat bij COVID-19 patiënten VTE vaker voorkomt dan bij andere ziektebeelden. Denk er bij onverklaarde symptomen, met name bij oudere patiënten, dus laagdrempelig aan. Blijf daarbij vasthouden aan evidence based medicine: vooralsnog zijn er in deze patiëntengroep geen andere afkapwaarden voor D-dimeer gevalideerd en wordt vanuit het RIVM geadviseerd de conventionele beslisregels ten aanzien van aanvullende beeldvorming te volgen.
Tot slot, de huidige tromboseprofylaxe richtlijnen kunnen (nog) niet met studies onderbouwd worden: blijf hierover per individuele patiënt een zorgvuldige afweging maken.

DISCLAIMER
Over COVID-19 verschijnen regelmatig nieuwe inzichten en zijn bestaande inzichten aan verandering onderhevig. Wij hebben ten tijde van het schrijven van deze post getracht de meest recente literatuur overzichtelijk samen te vatten. Het is raadzaam om bij specifieke vragen/beleidsmatige keuzes de laatste richtlijnen van het RIVM, SWAB en beroepsverenigingen te volgen.
Lees ook onze andere posts over COVID-19
Auteur: Gaby van den Wittenboer, ANIOS IC Martini Ziekenhuis (eerder: ANIOS SEH Isala)
Reviewer: Klaartje Caminada en Britt van der Kolk, SEH-artsen KNMG Isala
Literatuur
1. Horne JR, Vohl MC. Biological plausibility for interactions between dietary fat, resveratrol, ACE2 and SARS-CoV illness severity. Am J Physiol Endocrinol Metab. 2020. doi: 10.1152/ajpendo.00150.2020 [doi].
2. Wahedi HM, Ahmad S, Abbasi SW. Stilbene-based natural compounds as promising drug candidates against COVID-19. J Biomol Struct Dyn. 2020:1-16. doi: 10.1080/07391102.2020.1762743 [doi].
3. Wu C, Chen X, Cai Y, et al. Risk factors associated with acute respiratory distress syndrome and death in patients with coronavirus disease 2019 pneumonia in wuhan, china. JAMA Intern Med. 2020. https://doi.org/10.1001/jamainternmed.2020.0994. Accessed 4/23/2020. doi: 10.1001/jamainternmed.2020.0994.
4. Wang D, Hu B, Hu C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel Coronavirus–Infected pneumonia in wuhan, china. JAMA. 2020;323(11):1061-1069. https://doi.org/10.1001/jama.2020.1585. Accessed 4/21/2020. doi: 10.1001/jama.2020.1585.
5. Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in wuhan, china: A retrospective cohort study. The Lancet. 2020;395(10229):1054-1062. http://dx.doi.org/10.1016/S0140-6736(20)30566-3. doi: 10.1016/S0140-6736(20)30566-3.
6. Chen T, Wu D, Chen H, et al. Clinical characteristics of 113 deceased patients with coronavirus disease 2019: Retrospective study. BMJ. 2020;368:m1091. http://www.bmj.com/content/368/bmj.m1091.abstract. doi: 10.1136/bmj.m1091.
7. Tang N, Li D, Wang X, Sun Z. Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. Journal of thrombosis and haemostasis : JTH. 2020;18(4):844-847. https://pubmed.ncbi.nlm.nih.gov/32073213 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7166509/. doi: 10.1111/jth.14768.
8. Xie Y, Wang X, Yang P, Zhang S. COVID-19 complicated by acute pulmonary embolism. Radiology: Cardiothoracic Imaging. 2020;2(2):e200067. https://doi.org/10.1148/ryct.2020200067. doi: 10.1148/ryct.2020200067.
9. Danzi GB, Loffi M, Galeazzi G, Gherbesi E. Acute pulmonary embolism and COVID-19 pneumonia: A random association? Eur Heart J. 2020. https://doi.org/10.1093/eurheartj/ehaa254. doi: 10.1093/eurheartj/ehaa254.
10. Rotzinger DC, Beigelman-Aubry C, von Garnier C, Qanadli SD. Pulmonary embolism in patients with COVID-19: Time to change the paradigm of computed tomography. Thromb Res. 2020;190:58-59. https://pubmed.ncbi.nlm.nih.gov/32302782 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7151364/. doi: 10.1016/j.thromres.2020.04.011.
11. Klok FA, Kruip, M J H A., van der Meer, N. J. M., et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res. 2020:S0049-1. https://pubmed.ncbi.nlm.nih.gov/32291094 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7146714/. doi: 10.1016/j.thromres.2020.04.013.
12. Lim W, Meade M, Lauzier F, et al. Failure of anticoagulant thromboprophylaxis: Risk factors in medical-surgical critically ill patients*. Crit Care Med. 2015;43(2):401-410. doi: 10.1097/CCM.0000000000000713 [doi].
13. Malato A, Dentali F, Siragusa S, et al. The impact of deep vein thrombosis in critically ill patients: A meta-analysis of major clinical outcomes. Blood transfusion = Trasfusione del sangue. 2015;13(4):559-568. https://pubmed.ncbi.nlm.nih.gov/26513770 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4624530/. doi: 10.2450/2015.0277-14.
14. Klok FA, Kruip, M J H A., van der Meer, N. J. M., et al. Confirmation of the high cumulative incidence of thrombotic complications in critically ill ICU patients with COVID-19: An updated analysis. Thromb Res. 2020:S0049-2. https://pubmed.ncbi.nlm.nih.gov/32381264 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7192101/. doi: 10.1016/j.thromres.2020.04.041.
15. Middeldorp S, Coppens M, van Haaps TF, et al. Incidence of venous thromboembolism in hospitalized patients with COVID-19. Preprints. 2020(2020040345). doi: 10.20944/preprints202004.0345.v1.
16. Cui S, Chen S, Li X, Liu S, Wang F. Prevalence of venous thromboembolism in patients with severe novel coronavirus pneumonia. J Thromb Haemost. 2020;n/a. https://doi.org/10.1111/jth.14830. doi: 10.1111/jth.14830.
17. ZAKAI NA, McCLURE LA. Racial differences in venous thromboembolism. Journal of Thrombosis and Haemostasis. 2011;9(10):1877-1882. https://doi.org/10.1111/j.1538-7836.2011.04443.x. doi: 10.1111/j.1538-7836.2011.04443.x.
18. Julien P, Julien G, Morgan C, et al. Pulmonary embolism in COVID-19 patients: Awareness of an increased prevalence. Circulation. ;0(0). https://doi.org/10.1161/CIRCULATIONAHA.120.047430. doi: 10.1161/CIRCULATIONAHA.120.047430.
19. Helms J, Tacquard C, Severac F, et al. High risk of thrombosis in patients in severe SARS-CoV-2 infection: A multicenter prospective cohort study. Intensive Care Medicine. 2020. doi: 10.1007/s00134-020-06062-x.
20. Llitjos J, Leclerc M, Chochois C, et al. High incidence of venous thromboembolic events in anticoagulated severe COVID-19 patients. J Thromb Haemost. 2020;n/a. https://doi.org/10.1111/jth.14869. doi: 10.1111/jth.14869.
21. Marone EM, Rinaldi LF. Upsurge of deep venous thrombosis in patients affected by COVID-19: Preliminary data and possible explanations. Journal of Vascular Surgery: Venous and Lymphatic Disorders. 2020. http://www.sciencedirect.com/science/article/pii/S2213333X20302146. doi: https://doi.org/10.1016/j.jvsv.2020.04.004 “.
22. Lodigiani C, Iapichino G, Carenzo L, et al. Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in milan, italy. Thromb Res. 2020;191:9-14. https://pubmed.ncbi.nlm.nih.gov/32353746 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7177070/. doi: 10.1016/j.thromres.2020.04.024.
23. Cattaneo M, Bertinato EM, Birocchi S, et al. Pulmonary embolism or pulmonary thrombosis in COVID-19? is the recommendation to use high-dose heparin for thromboprophylaxis justified? Thromb Haemost. . doi: 10.1055/s-0040-1712097.
24. Grillet F, Behr J, Calame P, Aubry S, Delabrousse E. Acute pulmonary embolism associated with COVID-19 pneumonia detected by pulmonary CT angiography. Radiology. 2020:201544. https://doi.org/10.1148/radiol.2020201544. doi: 10.1148/radiol.2020201544.
25. Leonard-Lorant I, Delabranche X, Severac F, et al. Acute pulmonary embolism in COVID-19 patients on CT angiography and relationship to D-dimer levels. Radiology. 2020:201561. https://doi.org/10.1148/radiol.2020201561. doi: 10.1148/radiol.2020201561.
26. Bĕlohlávek J, Dytrych V, Linhart A. Pulmonary embolism, part I: Epidemiology, risk factors and risk stratification, pathophysiology, clinical presentation, diagnosis and nonthrombotic pulmonary embolism. Experimental and clinical cardiology. 2013;18(2):129-138. https://pubmed.ncbi.nlm.nih.gov/23940438 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3718593/.
27. Turetz M, Sideris AT, Friedman OA, Triphathi N, Horowitz JM. Epidemiology, pathophysiology, and natural history of pulmonary embolism. Seminars in interventional radiology. 2018;35(2):92-98. https://pubmed.ncbi.nlm.nih.gov/29872243 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5986574/. doi: 10.1055/s-0038-1642036.
28. Tom van der Poll and Marcel Levi. Crosstalk between inflammation and coagulation: The lessons of sepsis. Current Vascular Pharmacology. 2012;10(5):632-638. http://www.eurekaselect.com/node/100755/article. doi: http://dx.doi.org/10.2174/157016112801784549.
29. Jackson SP, Darbousset R, Schoenwaelder SM. Thromboinflammation: Challenges of therapeutically targeting coagulation and other host defense mechanisms. Blood. 2019;133(9):906-918. doi: 10.1182/blood-2018-11-882993 [doi].
30. Marcel L, van der PT, Büller Harry R. Bidirectional relation between inflammation and coagulation. Circulation. 2004;109(22):2698-2704. https://doi.org/10.1161/01.CIR.0000131660.51520.9A. doi: 10.1161/01.CIR.0000131660.51520.9A.
31. Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in wuhan, china. The Lancet. 2020;395(10223):497-506. https://doi.org/10.1016/S0140-6736(20)30183-5. doi: 10.1016/S0140-6736(20)30183-5.
32. Qin C, Zhou L, Hu Z, et al. Dysregulation of immune response in patients with COVID-19 in wuhan, china. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 2020:ciaa248. https://pubmed.ncbi.nlm.nih.gov/32161940 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7108125/. doi: 10.1093/cid/ciaa248.
33. Levi M, van der Poll T. Coagulation and sepsis. Thromb Res. 2017;149:38-44. doi: S0049-3848(16)30619-3 [pii].
34. van Gorp, E. C. M., Suharti C, ten Cate H, et al. Review: Infectious diseases and coagulation disorders. J Infect Dis. 1999;180(1):176-186. https://doi.org/10.1086/314829. doi: 10.1086/314829.
35. Escher R, Breakey N, Lämmle B. Severe COVID-19 infection associated with endothelial activation. Thrombosis research. 2020;190:62. https://www.ncbi.nlm.nih.gov/pubmed/32305740. doi: 10.1016/j.thromres.2020.04.014.
36. Panigada M, Bottino N, Tagliabue P, et al. Hypercoagulability of COVID-19 patients in intensive care unit. A report of thromboelastography findings and other parameters of hemostasis. J Thromb Haemost. 2020;n/a. https://doi.org/10.1111/jth.14850. doi: 10.1111/jth.14850.
37. Subramaniam S, Scharrer I. Procoagulant activity during viral infections. Front Biosci (Landmark Ed). 2018;23:1060-1081. doi: 4633 [pii].
38. Varga Z, Flammer AJ, Steiger P, et al. Endothelial cell infection and endotheliitis in COVID-19. The Lancet. . https://doi.org/10.1016/S0140-6736(20)30937-5. doi: 10.1016/S0140-6736(20)30937-5.
39. Walls AC, Park Y, Tortorici MA, Wall A, McGuire AT, Veesler D. Structure, function, and antigenicity of the SARS-CoV-2 spike glycoprotein. Cell. 2020;181(2):281-292.e6. http://www.sciencedirect.com/science/article/pii/S0092867420302622. doi: https://doi.org/10.1016/j.cell.2020.02.058.
40. Liu Peter P, Alice B, David S, Hongliang L. The science underlying COVID-19: Implications for the cardiovascular system. Circulation. ;0(0). https://doi.org/10.1161/CIRCULATIONAHA.120.047549. doi: 10.1161/CIRCULATIONAHA.120.047549.
41. Mendoza-Torres E, Oyarzun A, Mondaca-Ruff D, et al. ACE2 and vasoactive peptides: Novel players in cardiovascular/renal remodeling and hypertension. Ther Adv Cardiovasc Dis. 2015;9(4):217-237. doi: 10.1177/1753944715597623 [doi].
42. Verdecchia P, Cavallini C, Spanevello A, Angeli F. The pivotal link between ACE2 deficiency and SARS-CoV-2 infection. Eur J Intern Med. 2020. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7167588/.
43. Thomas MC, Pickering RJ, Tsorotes D, et al. Genetic Ace2 deficiency accentuates vascular inflammation and atherosclerosis in the ApoE knockout mouse. Circ Res. 2010;107(7):888-897. doi: 10.1161/CIRCRESAHA.110.219279 [doi].
44. Kaiming W, Mahmoud G, Oudit Gavin Y. Angiotensin converting enzyme 2: A double-edged sword. Circulation. ;0(0). https://doi.org/10.1161/CIRCULATIONAHA.120.047049. doi: 10.1161/CIRCULATIONAHA.120.047049.
45. Imai Y, Kuba K, Rao S, et al. Angiotensin-converting enzyme 2 protects from severe acute lung failure. Nature. 2005;436(7047):112-116. doi: nature03712 [pii].
46. Oudit GY, Crackower MA, Backx PH, Penninger JM. The role of ACE2 in cardiovascular physiology. Trends Cardiovasc Med. 2003;13(3):93-101. doi: S1050173802002335 [pii].
47. Cordazzo C, Neri T, Petrini S, et al. Angiotensin II induces the generation of procoagulant microparticles by human mononuclear cells via an angiotensin type 2 receptor-mediated pathway. Thromb Res. 2013;131(4):e168-e174. https://doi.org/10.1016/j.thromres.2013.01.019. doi: 10.1016/j.thromres.2013.01.019.
48. Magro C, Mulvey JJ, Berlin D, et al. Complement associated microvascular injury and thrombosis in the pathogenesis of severe COVID-19 infection: A report of five cases. Translational research : the journal of laboratory and clinical medicine. 2020:S1931-0. https://pubmed.ncbi.nlm.nih.gov/32299776 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7158248/. doi: 10.1016/j.trsl.2020.04.007.
49. Yao XH, Li TY, He ZC, et al. A pathological report of three COVID-19 cases by minimally invasive autopsies. Zhonghua Bing Li Xue Za Zhi. 2020;49(0):E009. doi: 10.3760/cma.j.cn112151-20200312-00193 [doi].
50. Fox SE, Akmatbekov A, Harbert JL, Li G, Brown JQ, Vander Heide RS. Pulmonary and cardiac pathology in covid-19: The first autopsy series from new orleans. medRxiv. 2020:2020.04.06.20050575. http://medrxiv.org/content/early/2020/04/10/2020.04.06.20050575.abstract. doi: 10.1101/2020.04.06.20050575.
51. Luo W, Yu H, Gou J, et al. Clinical pathology of critical patient with novel coronavirus pneumonia (COVID-19). Preprints. 2020(2020020407). https://www.preprints.org/manuscript/202002.0407/v1.
52. Han H, Yang L, Liu R, et al. Prominent changes in blood coagulation of patients with SARS-CoV-2 infection. Clinical Chemistry and Laboratory Medicine (CCLM). 2020(0):20200188. https://www.degruyter.com/view/journals/cclm/ahead-of-print/article-10.1515-cclm-2020-0188/article-10.1515-cclm-2020-0188.xml. doi: https://doi.org/10.1515/cclm-2020-0188.
53. Guan W, Ni Z, Hu Y, et al. Clinical characteristics of coronavirus disease 2019 in china. N Engl J Med. 2020. https://doi.org/10.1056/NEJMoa2002032. doi: 10.1056/NEJMoa2002032.
54. Brady L. Stein. Coagulopathy associated with COVID-19. NEJM Journal Watch. Oncology and Hematology. 2020. https://search.proquest.com/docview/2386747209. doi: 10.1056/nejm-jw.NA51254.
55. Fogarty H, Townsend L, Ni Cheallaigh C, et al. COVID-19 coagulopathy in caucasian patients. Br J Haematol. 2020;n/a. https://doi.org/10.1111/bjh.16749. doi: 10.1111/bjh.16749.
56. Saba L, Sverzellati N. Is COVID evolution due to occurrence of pulmonary vascular thrombosis? J Thorac Imaging. 9000;Publish Ahead of Print. https://journals.lww.com/thoracicimaging/Fulltext/9000/Is_COVID_Evolution_Due_to_Occurrence_of_Pulmonary.99419.aspx.
57. Tang N, Bai H, Chen X, Gong J, Li D, Sun Z. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Thromb Haemost. 2020;n/a. https://doi.org/10.1111/jth.14817. doi: 10.1111/jth.14817.
58. Ranucci M, Ballotta A, Di Dedda U, et al. The procoagulant pattern of patients with COVID-19 acute respiratory distress syndrome. J Thromb Haemost. 2020;n/a. https://doi.org/10.1111/jth.14854. doi: 10.1111/jth.14854.
59. Huisman M, Coppens M, Eikenboom J, et al. Leidraad COVID-19 coagulopathie. .
60. Oudkerk M, Büller H,R., Kuijpers D, et al. Diagnosis, prevention, and treatment of thromboembolic complications in COVID-19: Report of the national institute for public health of the netherlands. Radiology. 2020:201629. https://doi.org/10.1148/radiol.2020201629. doi: 10.1148/radiol.2020201629.
61. Chen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in wuhan, china: A descriptive study. The Lancet. 2020;395(10223):507-513. https://doi.org/10.1016/S0140-6736(20)30211-7. doi: 10.1016/S0140-6736(20)30211-7.



Recente reacties