Inleiding
Op de SEH komen frequent patiënten met dyspnoe. Er zijn verschillende ziektebeelden die acute dyspnoe kunnen veroorzaken: o.a. longembolie, pneumonie, pneumothorax en longoedeem. Het echografisch in beeld brengen van de (artefacten van de) longen, het hart en de vena cava inferior (VCI) levert ons snel extra informatie op. Longechografie en echocardiografie zijn een waardevol onderdeel van de point-of-care ultrasound (POCUS). De kennis van artefacten is zeer belangrijk tijdens echografie van de longen. In deze blogpost zal de basale techniek van longechografie, alveloaire consolidatie en pleurale effusie worden besproken. In een eerdere blogpost van fanofEM op 12 december 2017 werden de basisprincipes van longechografie reeds besproken (o.a. A-lijnen, reverberatie, B-lijnen, lungsliding, lungpulse, lungpoint en comet tails).
Techniek longechografie
De lineaire probe (hoge frequentie) kan worden gebruikt voor het beoordelen van de pleura. Voor de overige beoordeling van de longartefacten kan het beste gebruik worden gemaakt van de curvedlineair of phased array probe (lage frequentie). Een maximale diepte van 4-6 cm is gebruikelijk voor een optimale beoordeling van de pleura en de bijbehorende artefacten. De overige onderdelen (exclusief pleura) kunnen op een diepte van ten minste 15 cm pas goed worden beoordeeld.
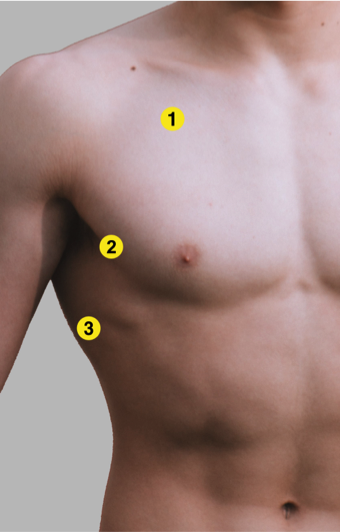
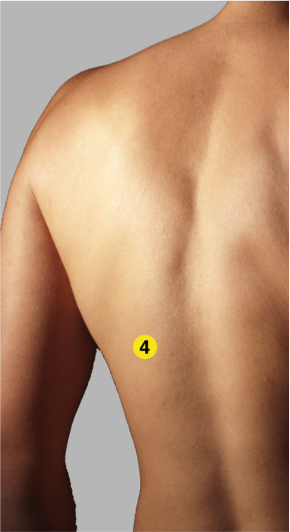
De thorax kan het beste op een gestructureerde manier worden bekeken, dit wordt bereikt door beide zijden van de thorax op (minimaal) vier verschillende punten te bekijken (zie de onderstaande twee foto’s). Pleurale effusie (sensitiviteit 90% en specificiteit 98%) en/of een consolidatie (sensitiviteit 42% en specificiteit 96%) kan in het posterolateraal alveolair pleurasyndroom (PLAPS)-punt worden gezien.
Punt 1. Mid-claviculaire lijn ter plaatse van de 2de intercostaal ruimte
Punt 2. Antero-axillaire lijn ter plaatse van de 5de intercostaal ruimte
Punt 3. Mid-axillaire lijn ter plaatse van het diafragma
Punt 4. Posterolateraal alveolair pleurasyndroom (PLAPS)- point, het meest posterieure punt boven het diafragma
Protocollen
Er zijn tal van protocollen (o.a. BLUE, FALLS) waarin de longen op een systematische wijze echografisch in beeld worden gebracht. Elk protocol heeft zo zijn voor en nadelen. Het uitgangspunt is dat er op een gestructureerde manier naar de longen gekeken wordt daarnaast is kennis van artefacten van belang om pathologie te herkennen.
Consolidatie
Meerdere artefacten tijdens longechografie kunnen wijzen op de aanwezigheid van een alveolaire consolidatie:
B-lijnen
Een ‘natte’ long bevat B-lijnen, dit zijn verticaal verlopende (lijnen) artefacten door reverberatie met een lengte van minstens 15-20 cm (zie video 1). B-lijnen worden pas pathologisch beschouwd wanneer er 3 of meer in twee of meer intercostaal ruimten worden gezien. Een B-lijn hoeft dus niet pathologisch te zijn, bijvoorbeeld in het geval van een longfissuur. B-lijnen ontstaan wanneer geluidsgolven heen en weer worden gekaatst tussen vocht, dat zich tussen verwijde interlobulaire septa bevindt, en de met lucht gevulde alveoli. Er worden lange, hyperechoïsche (wit van kleur), laserachtige, lijnen tot aan de bodem van het beeld gezien. Een B-lijn beweegt met de ademhaling en dus met de lungsliding mee. Bij onder andere een pneumonie, decompensatio cordis, ARDS en interstitiële longaandoeningen (zoals longfibrose) worden B-lijnen gezien. Een beginnende (eenzijdige pneumonie) kenmerkt zich door B-lijnen. In de contralaterale long worden A-lijnen gezien passende bij een ‘droge long’, normale long (zie video 2).
Video 1: B-lijnen
Video 2: A-lijnen
Subpleurale consolidatie
Bij een pneumonie kan men in een vroeg stadium subpleurale consolidaties aantreffen. Het kenmerkt zich door een kleine vochtcollectie (hypo-echogeen, zwart van kleur) onder de pleura. Naast een bacteriële pneumonie kunnen subpleurale consolidaties ook een andere oorzaak hebben, zoals bijvoorbeeld een longinfarct bij een longembolieën.
Hepatisatie
Het longparenchym van een gevorderde pneumonie vertoont echografische kenmerken van de lever, dit fenomeen wordt ook wel hepatisatie genoemd (zie video 3 en 4). Een ander kenmerk van een pneumonie is dat het een groot gedeelte van de long inneemt zonder volume verlies.
Video 3: consolidatie van de long
Video 4: hepatisatie
Shred sign
Een hyperechogene irregulaire lijn is zichtbaar tussen een gedeelte van de long met een consolidatie (niet-beluchte longgedeelte) en gezond longweefsel (zie video 5).
Luchtbronchogram
Een dynamisch luchtbronchogram komt frequent voor bij gevorderde pneumonie, dit is een beweegbaar, hyperechogeen, puntvormig gebied die beweegt tijdens de ademhaling (zie video 6). De oorzaak van dit verschijnsel is dat lucht wordt ingesloten in een bronchi door het infiltraat.
Video 5: shred sign
Video 6: statisch- en dynamisch lunchtbronchogram
Atelectase
Een atelectase kenmerkt zich door samengedrukte alveoli. Het wordt frequent gezien bij beademde patiënten door hypoinflatie en proximale bronchusobstructie. Een ander kenmerk is een statisch luchtbronchogram, een niet beweegbaar, hyperechogeen, puntvormige gebied dat niet beweegt tijdens de ademhaling. Echter, het kan ook in 40% van de patiënten met een pneumonie worden gezien. Een pneumonie zal eerder een dynamisch luchtbronchogram vertonen zonder veel volumverlies terwijl een atelectase doorgaans een statisch luchtbronchogram laat zien met volumeverlies (zie video 6).
Pleurale effusie
Pleurale effusie kan het beste met de curved linear probe (lage frequentie) worden bekeken. Op ongeveer 0,5 cm onder de ribben bevindt zich de pleura. Echografisch kenmerkt zich een pleurale effusie meestal anechoïsch (zwart van kleur) tussen de pleura pariëtalis en visceralis (zie video 7). Uit onderzoek is gebleken dat echografie al 3-5 ml pleurale effusie kan detecteren. In vergelijking met een CT-scan van de thorax heeft echo een sensitiviteit en specificiteit van ongeveer 93% voor het aantonen van een pleurale effusie. Het ‘spine sign’ is een indirecte indicator voor de aanwezigheid van een pleurale effusie of hematothorax. Kenmerkend voor het ‘spine sign’ is het echografisch in beeld krijgen van wervels die craniaal van het diafragma doorlopen in de thoraxholte (zie video 7).
Video 7: pleuravocht en “spine sign”
Het is belangrijk om de volgende drie factoren te identificeren om de aanwezigheid van een pleurale effusie te bevestigen:
- Anatomie: herkennen van de lever, milt, diafragma, lever, ribben en het longparenchym
- Anechoïesche afwijking: een pleurale effusie wordt omgeven door een typische anatomische begrenzing
- Dynamische veranderingen: beweging van de longen en diafragma in een pleurale effusie ‘ook wel ” lung flapping” of “jellyfish” genoemd (zie video 8).
Het niet goed kunnen visualiseren van diepere structuren door het bewegen van normaal geventileerd longweefsel door de ademhalingscyclus wordt het ‘curtain sign’ genoemd (zie video 9). Dit is het beeld dat bij een normale luchthoudende long met de phased array probe wordt gezien ter hoogte van de sinus pleura.
Video 8: “fishtail” sign / “jellyfish” sign
Video 9: “curtain” sign
PEARLS & PITFALLS
- Combineer longechografie bij een patiënt met dyspnoe met echocardiografie en echo van de VCI.
- Bekijk de thorax, zowel links als rechts, op minimaal vier verschillende punten.
- Aanwezigheid van A-lijnen betekent geen vocht, pneumonie, longcontusie of longoedeem op de onderzochte plek.
- B-lijnen zijn pathologisch wanneer er 3 of meer in twee of meer aaneengesloten intercostaal ruimten worden gezien (o.a. bij longoedeem (bilateraal), pneumonie (meestal unilateraal), interstitiële longziekte).
- PLAPS: pleurale effusie en een alveolaire consolidatie kan men vaak hier aantonen dan wel uitsluiten.
- Een minimale hoeveelheid van 5 ml pleurale effusie of hematothorax kan indirect worden aangetoond met het “spine sign”.
- Hepatisatie: longparenchym vertoont echografische kenmerken van een lever, past bij een consolidatie.
- Correleer altijd de echo bevindingen aan de kliniek van de patiënt!
Meer lezen?
fanofEM
- De basisprincipes van longechografie
- Point-of-care echografie bij patiënten met respiratoire symptomen op de SEH
Life in the Fastlane
5 Min Sono
- Pneumonie http://5minsono.com/pna/
- Pleurale effusie http://5minsono.com/pleuraleffusions/
- Metingen pleurale effusie http://5minsono.com/pleuraleffusions2/
- Longembolie http://5minsono.com/5-second-sono-pulmonary-embolism/
Western Sono
- Consolidatie https://westernsono.ca/screencasts/lung-ultrasound/alveolar-consolidation-and-shred-sign-2/
SGEM
The Pocus Atlas
- Longechografie http://www.thepocusatlas.com/ea-pulm
NVSHA
Literatuur
- Lichtenstein DA, et al. Ultrasound diagnosis of alveolar consolidation in the critically ill. Intensive Care Med. 30:276-281 2004
- Vicki E. Noble, Bret P. Nelson. Manual of Emergency and Critical Care Ultrasound. Cambridge University Press. Jun 2011.
- Nilam J. Soni, Robert Arntfield, Pierre Kory. Point of Care Ultrasound. Elsevier Health Sciences. Aug 2014.
- Orso D, et al. Lung ultrasound in diagnosing pneumonia in childhood: a systematic review and meta-analysis. J Ultrasound. 2018 Jun 21.
- Balk DS, et al. Lung ultrasound compared to chest X-ray for diagnosis of pediatric pneumonia: A meta-analysis.Pediatr Pulmonol. 2018 Apr 26.
- Martindale JL, et al. Diagnosing Acute Heart Failure in the Emergency Department: A Systematic Review and Meta-analysis.Acad Emerg Med. 2016 Mar;23(3):223-42.
- Lichtenstein D. Fluid Administration Limited by Lung Sonography: the place of lung ultrasound in assessment of acute circulatory failure (the FALLS-protocol). Expert Rev Respir Med. 2012;6:155–162.
- Lichtenstein DA, et al. Relevance of lung ultrasound in the diagnosis of acute respiratory failure: the BLUE protocol. Chest. 2008 Jul;134(1):117-25.
- Lichtenstein D. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill. Chest. 2015 Jun;147(6):1659-1670.
- Dickman E, et al. Extension of the Thoracic Spine Sign: A New Sonographic Marker of Pleural Effusion. J Ultrasound Med. 2015 Sep;34(9):1555-61
- Pareda MA, et al. Lung ultrasound for the diagnosis of pneumonia in children: a meta-analysis. Pediatrics. 2015 Apr;135(4):714-22.
- Reissig A, et al. Lung ultrasound in community-acquired pneumonia and in interstitial lung diseases.Respiration. 2014;87(3):179-89.
- Chavez MA, et al. Lung ultrasound for the diagnosis of pneumonia in adults: a systematic review and meta-analysis.Respir Res. 2014 Apr 23;15:50.
- Lichtenstein D. Lung ultrasound in the critically ill. Curr Opin Crit Care. 2014 Jun;20(3):315-22.
- Volpicelli G, et al. International evidence-based recommendations for point-of-care lung ultrasound. Intensive Care Med (2012) 38:577–591.
Auteur: Joris Datema, SEH-arts KNMG
Reviewer: Vincent Rietveld, SEH-arts KNMG en Leonie Geut SEH-arts KNMG



Recente reacties